Siemens Healthineers MedMuseum
Geschichte(n) entdecken
- „Ich habe mich sozusagen verloren“
„Ich habe mich sozusagen verloren“
Alois Alzheimer schildert 1906 in einem Vortrag die Vorgeschichte seiner Patientin Auguste Deter, die 1901 in die „Anstalt für Irre und Epileptische“ in Frankfurt am Main eingeliefert wurde, an der er als Oberarzt tätig war. Er beschreibt die typischen frühen Anzeichen einer Alzheimer-Demenz wie Gedächtnisverlust, Orientierungsprobleme sowie Verhaltens- und Persönlichkeitsveränderungen. Schon oft hat Alzheimer diese Symptome bei Patienten*innen gesehen, aber bei Auguste Deter, wird er stutzig, denn sie ist erst 51 Jahre alt.
Deshalb beginnt er, die Patientin eingehend zu untersuchen. Neben der Feststellung des körperlichen Allgemeinzustandes führt Alzheimer unterschiedliche kognitive Tests durch, die er akribisch in der Patientenakte dokumentiert. Die Basis sind Gespräche, die Alzheimer mit Auguste Deter führt und in denen er ihr verschiedene Aufgaben stellt. Zum Beispiel soll sie Gegenstände benennen oder einfache Rechen- und Schreibaufgaben lösen. Viele dieser Aufgaben sind auch heute noch Bestandteil von standardisierten kognitiven Tests zur Demenz-Früherkennung.
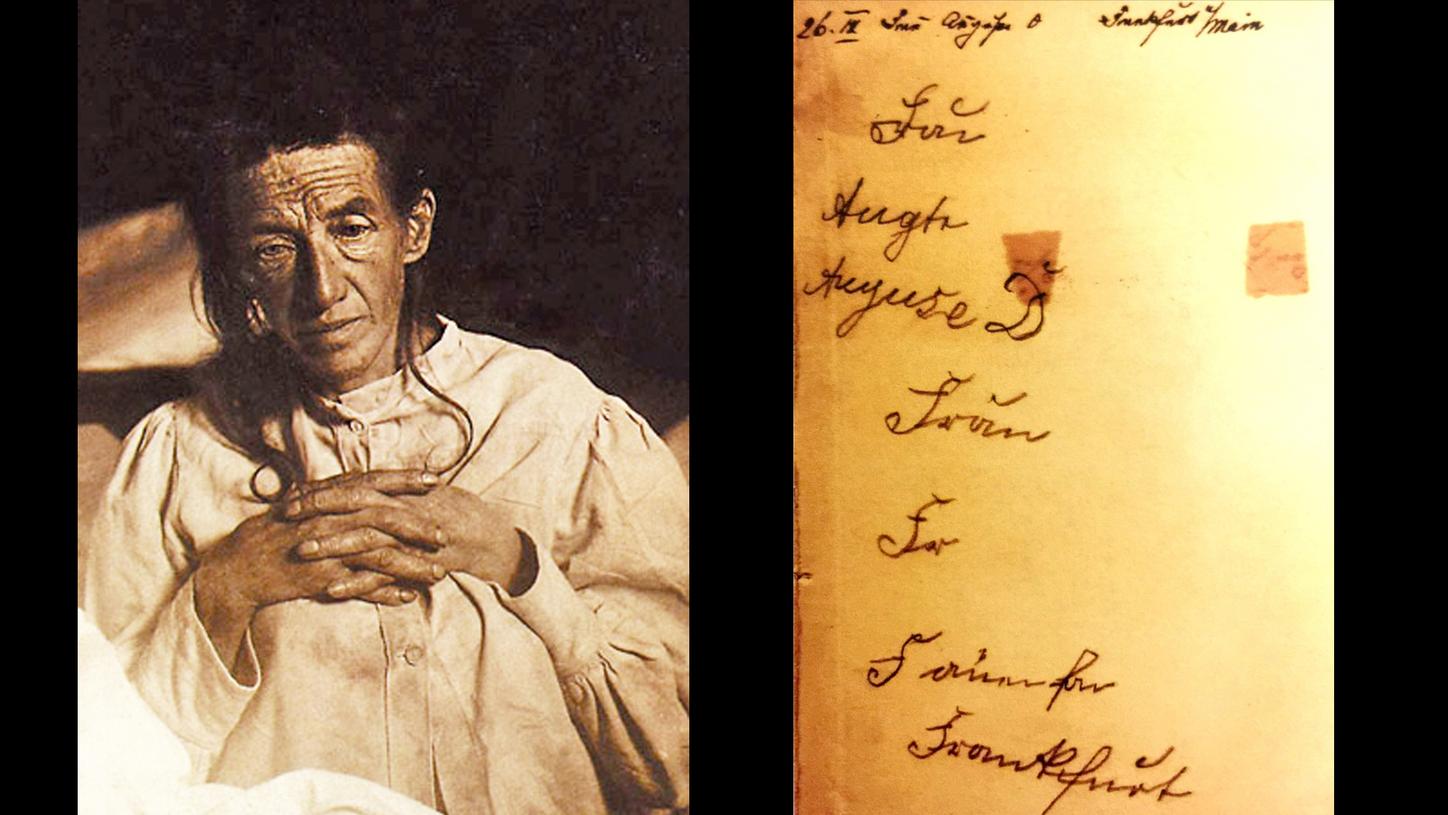
Portrait und Schriftprobe von Auguste Deter
Alois Alzheimer
Alois Alzheimer (born June 14, 1864, in Marktbreit; died December 19, 1915, in Breslau, now Wrocław) studied medicine at the University of Würzburg. After completing his studies, he took up a position as a resident physician at the “Institute for the Insane and Epileptic” in Frankfurt am Main in 1888, eventually becoming a senior physician in 1896. He moved first to Heidelberg in 1902 and then, in 1903, to the Royal Psychiatric Clinic in Munich, where he studied Deter’s brain. His final stop was Breslau, where he became director of the Neurologic and Psychiatric Institute of Friedrich Wilhelm University in 1912.
Was ist Demenz?
Demenz ist ein Oberbegriff für verschiedene Erkrankungen, die das Gehirn betreffen und zu Gedächtnis- und Denkstörungen führen. Alzheimer ist die häufigste Form der Demenz – zwischen 60 und 80 Prozent aller Menschen mit Demenz haben Alzheimer.
Außerdem bittet Alzheimer seine Patientin: „Schreiben Sie <Auguste D.>“. Sie schreibt „Frau“, den Rest hat sie inzwischen vergessen. Immer und immer wieder wiederholt Alzheimer ihren Namen. Anstelle von „Auguste“ schreibt sie „Auguse“. Es gelingt ihr einfach nicht mehr, ihren Namen vollständig aufzuschreiben. In einem klaren Moment erkennt Auguste: „Ich habe mich sozusagen verloren.“
Alzheimer vermutet, dass er einer neuen Krankheit auf der Spur ist. Tatsächlich gehört sie aber schon immer zum menschlichen Dasein. In der Antike beschreibt der römische Dichter Juvenal in einer seiner Satiren die Demenz als Schrecken des Alters:
Was aber noch weit erbärmlicher als die Gebrechlichkeit aller Glieder ist, das ist seine Blödsinnigkeit, die weder den Namen der Knechte, noch das Angesicht des Freundes kennet, mit dem er in letzter Nacht gespeiset, noch selbst die Kinder, die er gezeuget, die er auferzogen hat.
Decimus Junius Juvenalis, ca. 1. und 2. Jahrhundert n. Chr.
Den Ursachen auf der Spur
Lange Zeit wurden die Demenz-Symptome als Altersblödsinn abgetan und auch Alzheimer kann bei Auguste Deter zunächst nur die vorläufige Diagnose „Präseniles Irresein“ stellen. Doch er begnügt sich nicht mit dieser Diagnose und forscht weiter. Nach Augustes Tod untersucht Alzheimer ihr Gehirn im Labor und macht unter dem Mikroskop eine interessante Entdeckung: „Über die ganze Rinde zerstreut, besonders zahlreich in den oberen Schichten, findet man miliare Herdchen, welche durch die Einlagerung eines eigenartigen Stoffes in die Hirnrinde bedingt sind.“ Diesen „eigenartigen Stoff“ identifizieren George Glenner und Caine Wong 1984 als Ansammlung eines Eiweißstückchens mit dem Namen „Beta-Amyloid“. Doch woher kommen diese Proteinfragmente? Ein Forscherteam der Universität in Köln beantwortet 1987 die Frage und zeigt, dass Beta-Amyloid bei der Spaltung des Amyloid-Vorläuferproteins entsteht. Bei gesunden Menschen werden diese Eiweißstückchen durch Enzyme abgebaut und aus dem Gehirn abtransportiert. Hingegen ist bei Patient*innen, die an Alzheimer erkrankt sind, der Abbauprozess gestört, weshalb die Moleküle zwischen den Nervenzellen verbleiben und verklumpen - es entstehen sogenannte „Beta-Amyloid-Plaques“.
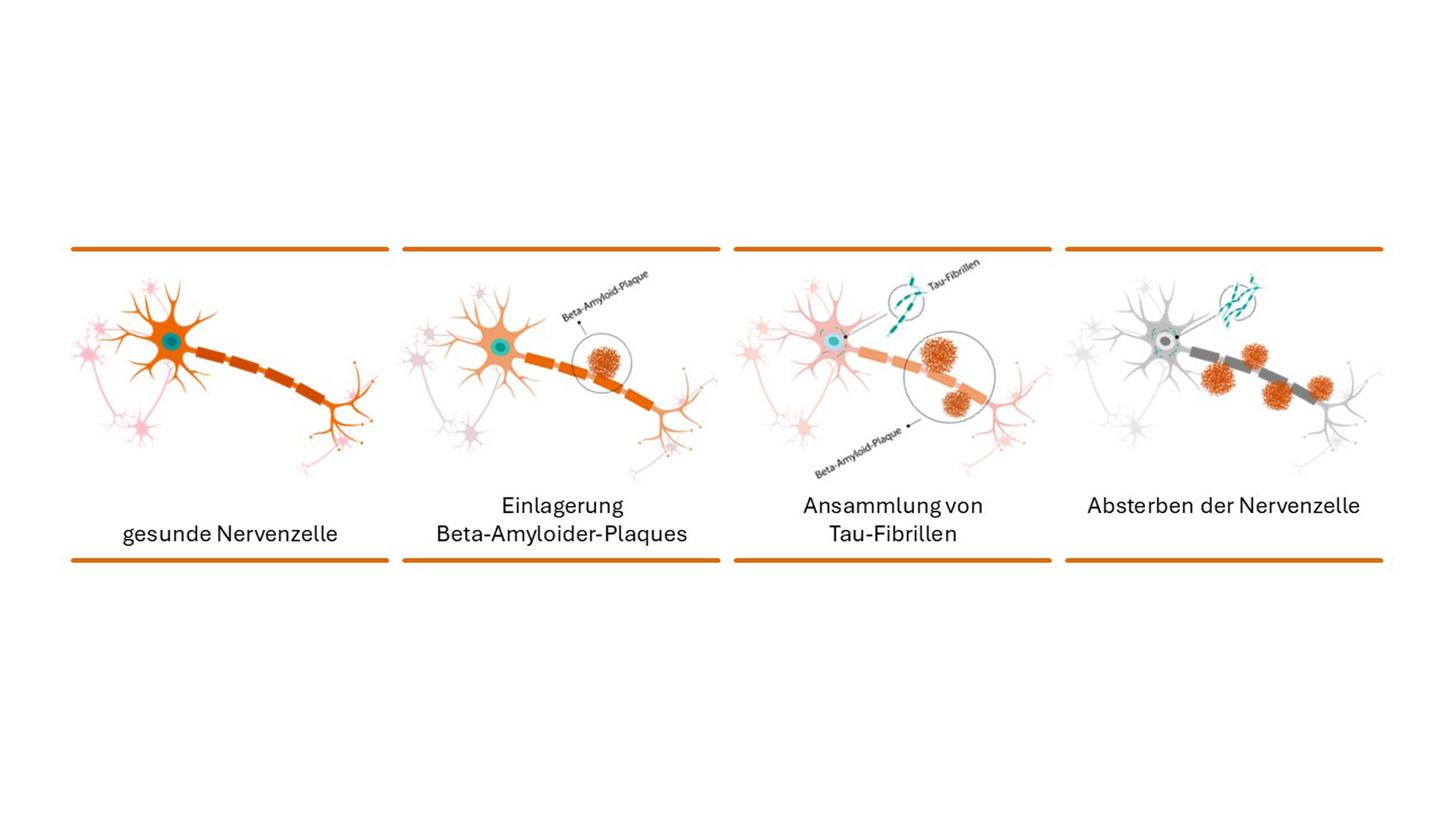
Darstellung der Nervenzellen in einem normalen Gehirn (links) und der Einlagerung Beta-Amyloider-Plaques und Tau-Fibrillen (Mitte) in einem Gehirn einer an Alzheimer erkrankten Person, die zum Absterben der Zelle führen (rechts).
Außerdem erkennt Alzheimer im Gehirn von Auguste Deter „merkwürdige Veränderungen der Neurofibrillen“, der Inge Grundke-Iqbal mit ihren Kollegen 80 Jahre später auf die Spur kommt. Neurofibrillen sind Fasern innerhalb der Gehirnzellen, die zur Aufrechterhaltung der Zellstruktur beitragen. Die Forschergruppe um Grundke-Iqbal findet heraus, dass das Tau-Protein eine Schlüsselkomponente der Neurofibrillen ist. Eigentlich stabilisiert das Tau-Protein die Transportwege im Gehirn. Bei Alzheimer-Patienten kommt es zu einer Fehlsteuerung und das Tau-Protein verfilzt zu Bündeln innerhalb der Nervenzellen, den sogenannten Tau-Fibrillen. Sowohl die Tau-Fibrillen als auch die Beta-Amyloid-Plaques sind wichtige Ursachen der Alzheimer Erkrankung, denn sie verhindern, dass die Nervenzellen miteinander kommunizieren können und sorgen dafür, dass sie langsam absterben. Warum sich diese Ablagerungen bilden, ist bis heute nicht geklärt.
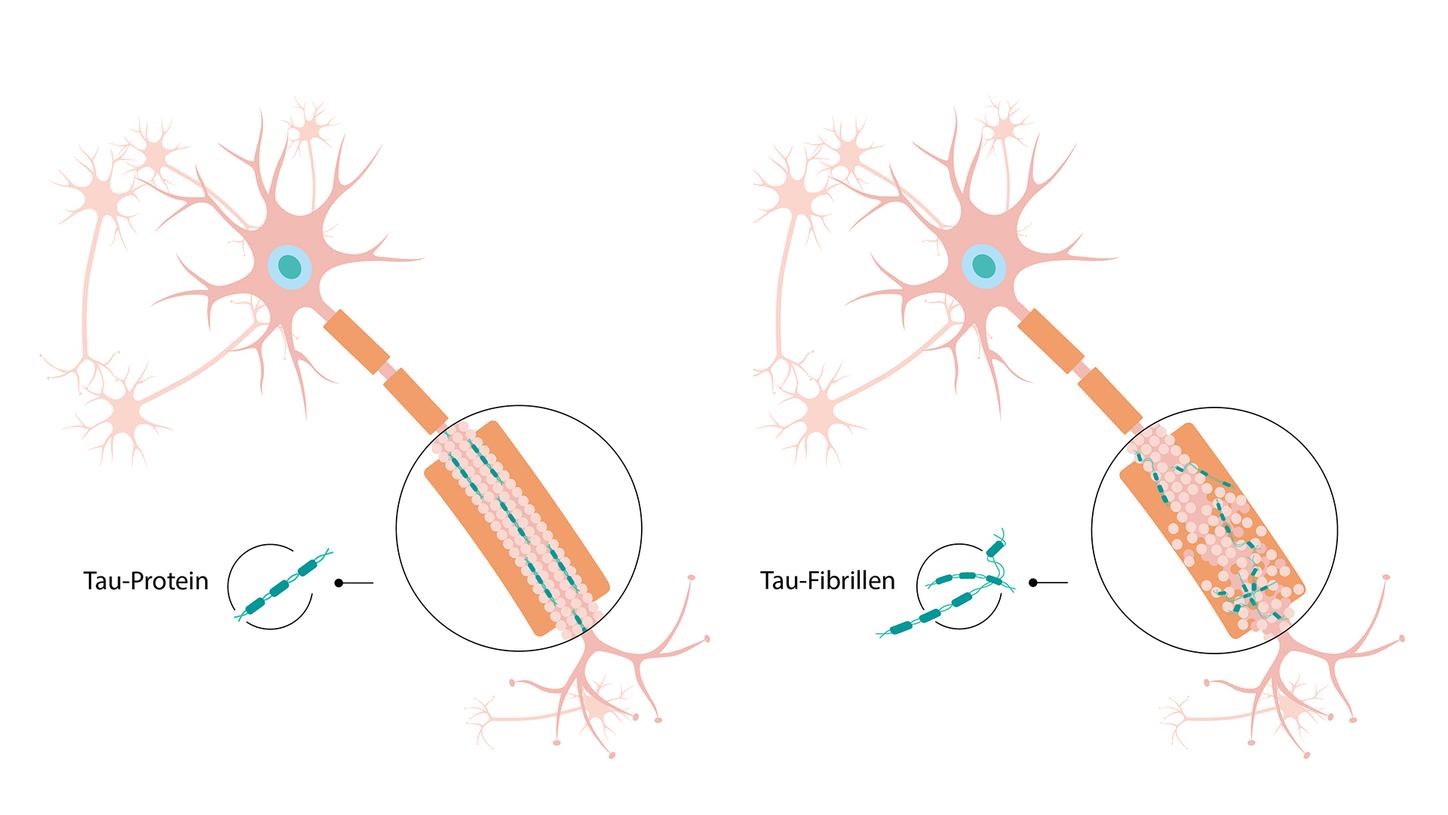
Vergleich einer gesunden Nervenzelle (links) und einer neuronalen Degeneration (rechts), bei der die Tau-Proteine (türkis) zu Tau-Fibrillen verklumpen, die sich innerhalb der Nervenzellen ansammeln.
Eine Hollywood-Diva wird Patientin
Die Erforschung der Alzheimer-Krankheit nimmt in den 1980er Jahren stetig Fahrt auf. Während die Krankheit lange Zeit als eine medizinische Seltenheit galt, tritt sie mit dem Anstieg der Lebenserwartung seit den 1960er Jahren immer häufiger auf. Umso älter die Menschen werden, umso größer ist das Risiko, an Alzheimer zu erkranken. Manchmal kann die Krankheit aber auch jüngere Menschen treffen, wie die Fälle von Auguste Deter oder Rita Hayworth zeigen, die beide mit Anfang 50 die ersten Symptome aufweisen.
Bei Rita Hayworth beginnt die Erkrankung Anfang der 1970er Jahre damit, dass sie am Set Dialoge vergisst und zu Stimmungsschwankungen neigt. Sind das vielleicht die typischen Allüren einer Hollywood-Diva? Als sich ihr Zustand verschlechtert und die amerikanische Schauspielerin orientierungslos durch Los Angeles irrt, vermutet man eine ausgeprägte Alkoholsucht. 1981 wird endlich die richtige Diagnose gestellt: Rita Hayworth leidet an Alzheimer. Plötzlich berichten die Medien von dieser Krankheit und sie rückt ins Bewusstsein der Öffentlichkeit.
Der Fall der Rita Hayworth zeigt, wie schwierig es noch in den 1980er Jahren ist, Alzheimer zu diagnostizieren. Letztlich kann man über ein aufwendiges Verfahren bestehend aus verschiedenen Untersuchungen und kognitiven Tests andere Krankheiten lediglich ausschließen. Weder im Blut noch in einer Computertomographie- oder Magnetresonanztomographie-Aufnahme gibt sich Alzheimer in einem frühen Stadium zu erkennen. Erst wenn es zu spät und das Gehirn krankheitsbedingt geschrumpft ist, kann man die Erkrankung im klinischen Bild sehen. Eine Möglichkeit für eine eindeutige Diagnose bahnt sich erst mit der Entwicklung der Positronen-Emissions-Tomographie (PET) und spezieller Tracer an. Außerdem kommt Mitte der 1990er Jahre der Liquortest als weitere Diagnosemöglichkeit hinzu, nachdem Forscher entdeckt haben, dass sich Alzheimer in der Gehirn-Rückenmark-Flüssigkeit nachweisen lässt. Beide Verfahren haben sich mittlerweile als Standardverfahren zur Früherkennung von Alzheimer etabliert und können mit Systemen von Siemens Healthineers durchgeführt werden.
Was ist PET und was sind Tracer?
Die Positronen-Emissions-Tomographie ist ein nuklearmedizinisches Verfahren, bei dem Stoffwechselaktivitäten im Körper sichtbar gemacht werden. Dazu wird Patient*innen ein sogenannter Tracer injiziert. Der Tracer ist eine leicht radioaktiv markierte Substanz wie zum Beispiel Traubenzucker, die am Stoffwechsel im Körper teilnimmt. Der PET-Scanner stellt dann die Verteilung des Tracers im Körper da.
Was ist ein Liquortest?
Für die Untersuchung wird den Patientin*innen über den Wirbelkanal Liquor (Gehirn-Rückenmark-Flüssigkeit) mit einer Kanüle entnommen. Anschließend erfolgt die Liquoranlyse im Labor mit Systemen wie Atellica® Solution. Die für die Alzheimer-Krankheit typischen Proteine, Amyloid-Beta und Tau, sind im Krankheitsfall im Liquor in veränderter Konzentration enthalten.
Entwicklung der Positronen-Emissions-Tomographie
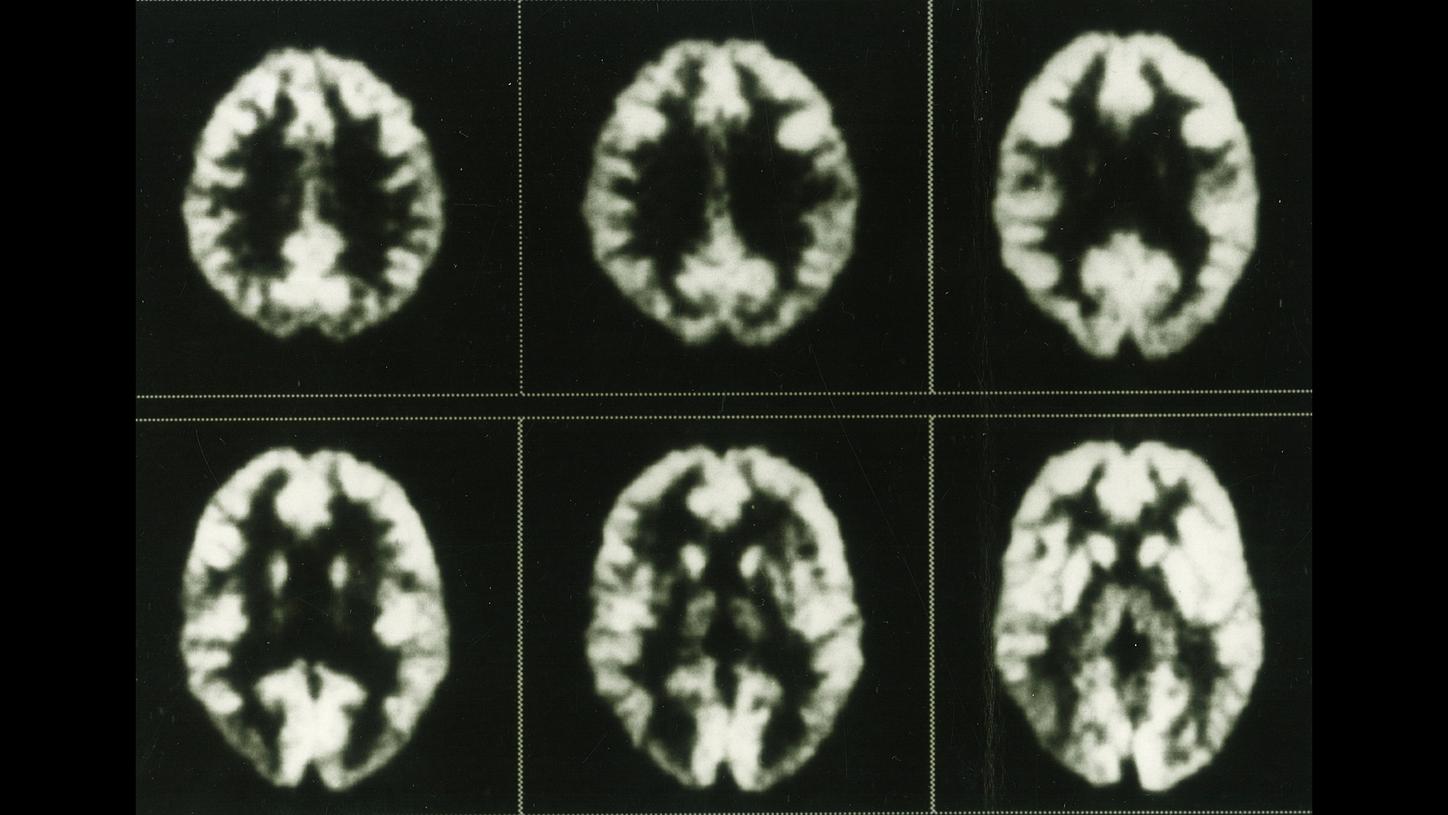
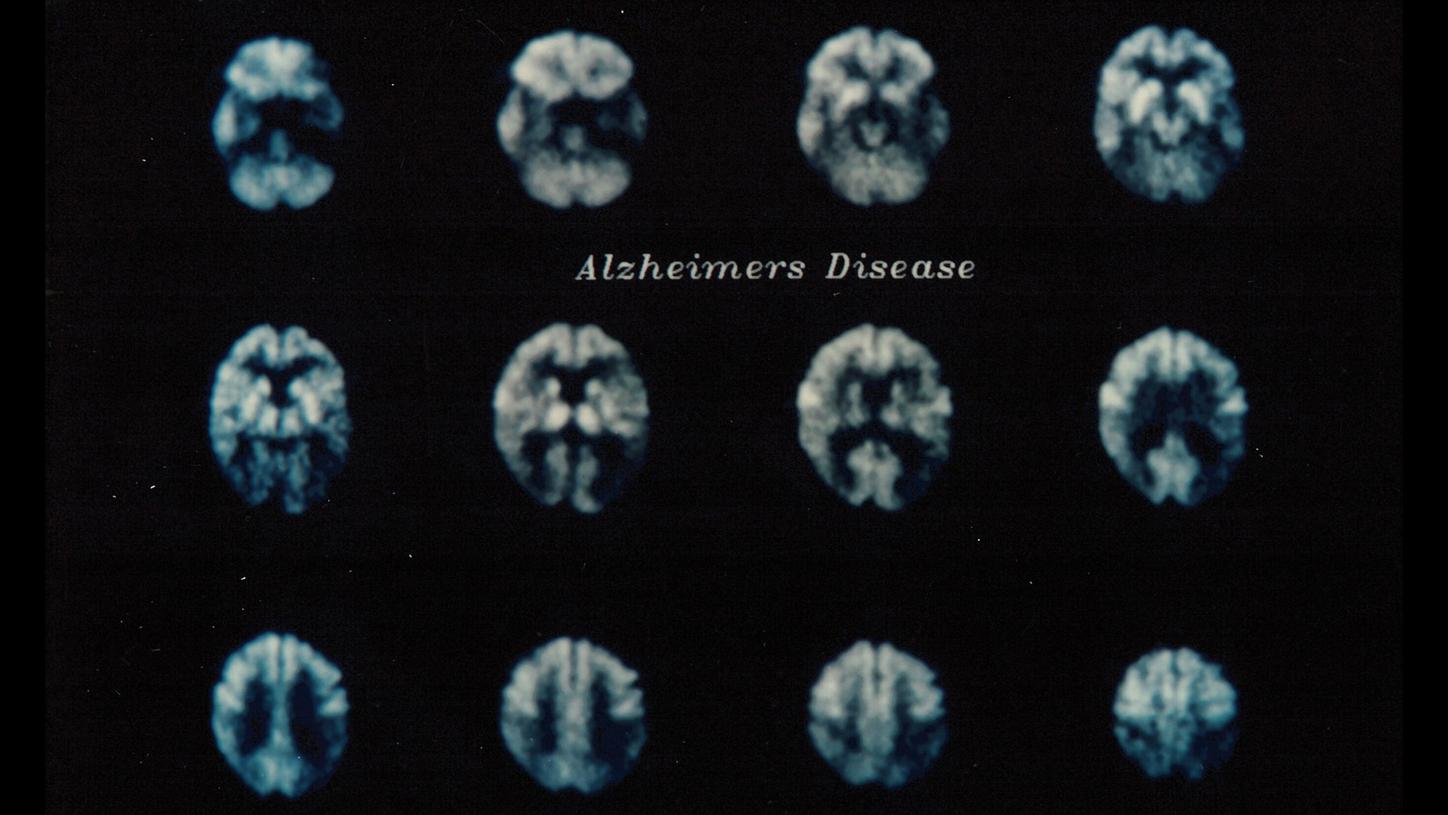
Anfang der 1970er Jahre werden die ersten PET-Scanner entwickelt. Bereits auf den frühen Aufnahmen mit den Prototypen ist der Glukose-Stoffwechsel im Gehirn zu erkennen. Auf dieser Bilderserie, aufgenommen mit dem ECAT III Mitte der 1980er Jahre, ist die Verteilung von Fluordesoxyglucose (FDG) in einem gesunden Gehirn zu sehen.
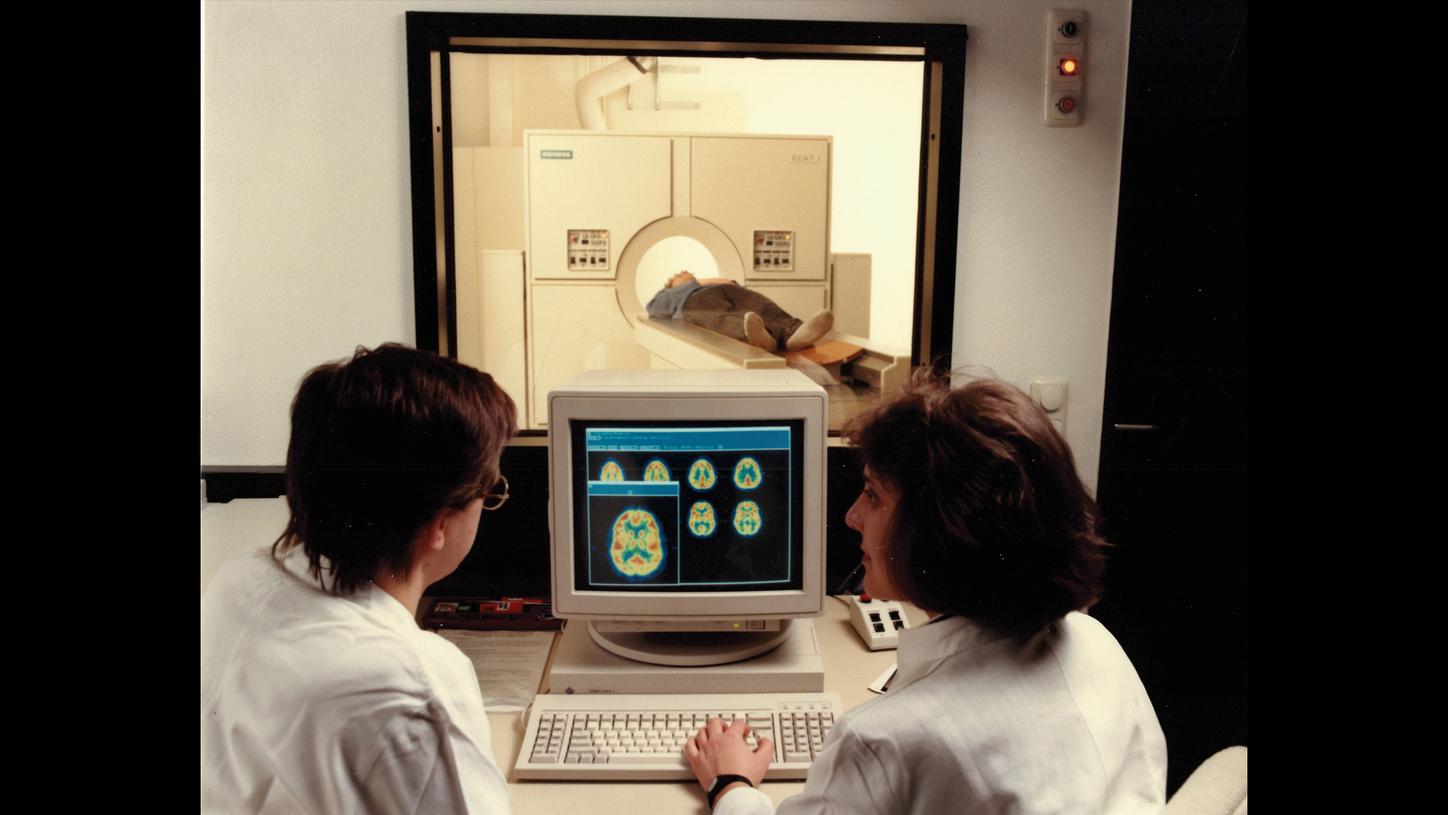
Ab den 1980er Jahren wird die PET auch zur Alzheimer-Diagnostik eingesetzt. Noch ist es aber kein Routine-Verfahren und wird vor allem zu Forschungszwecken genutzt.

Ende der 1980er Jahre ist die PET in erster Linie noch immer ein Mittel zur Forschung und kommt selten in Krankenhäusern zum Einsatz, denn es gibt nur wenige Zyklotrone, in denen die Tracer hergestellt werden können. Durch die Entwicklung kleiner, kostengünstiger Zyklotrone, können die Tracer schließlich direkt in den Kliniken produziert werden. Parallel dazu wird mit PETNET ein flächendeckendes Vertriebsnetz entwickelt, um die Tracer schnell in die Praxen liefern zu können.
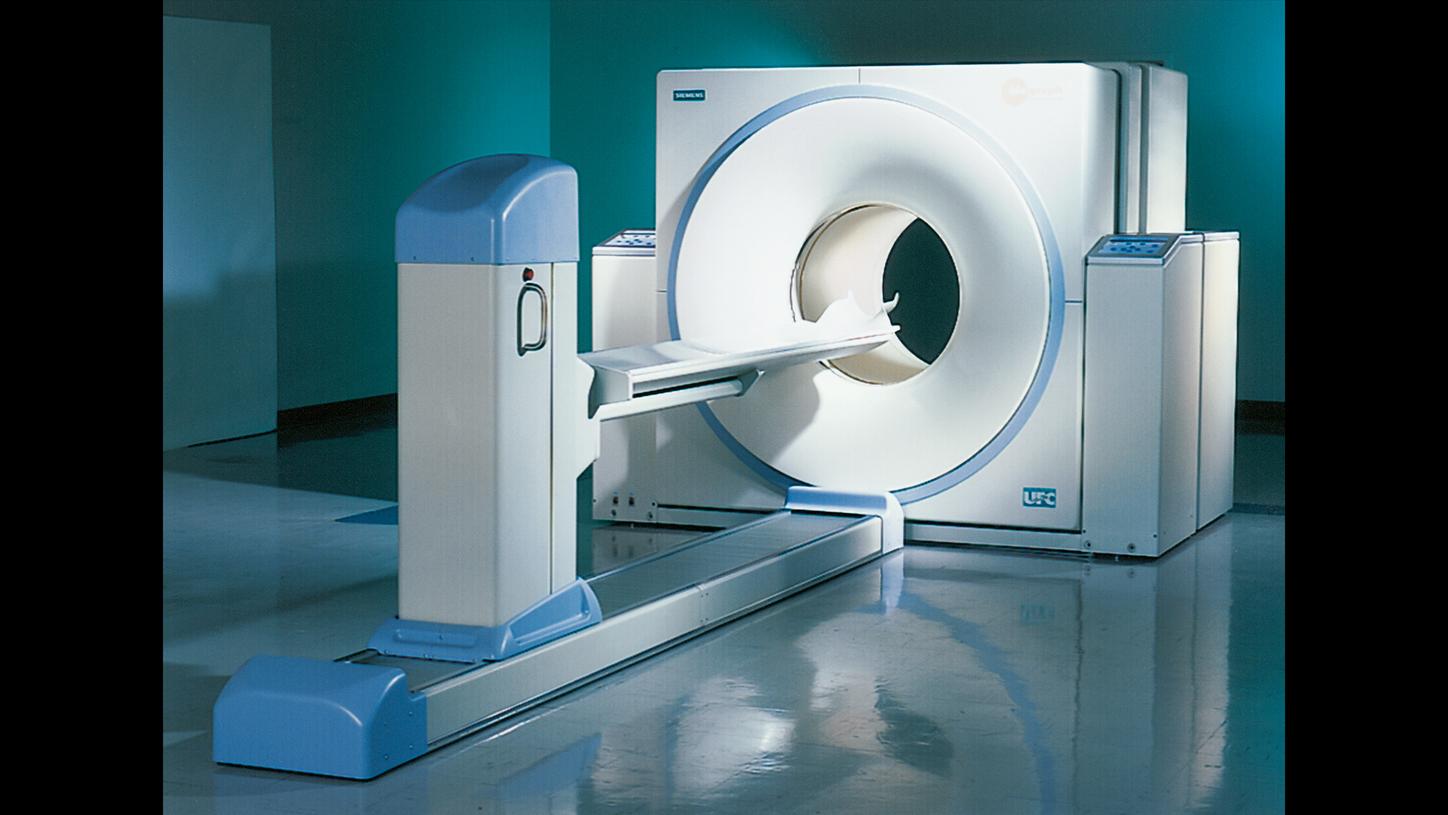
Die PET zeigt zwar den Stoffwechsel, nicht aber die Anatomie. Ab 2000 ist beides möglich, denn der Biograph vereint die Positronen-Emissions-Tomographie (PET) und Computertomographie (CT) in einem Gerät.
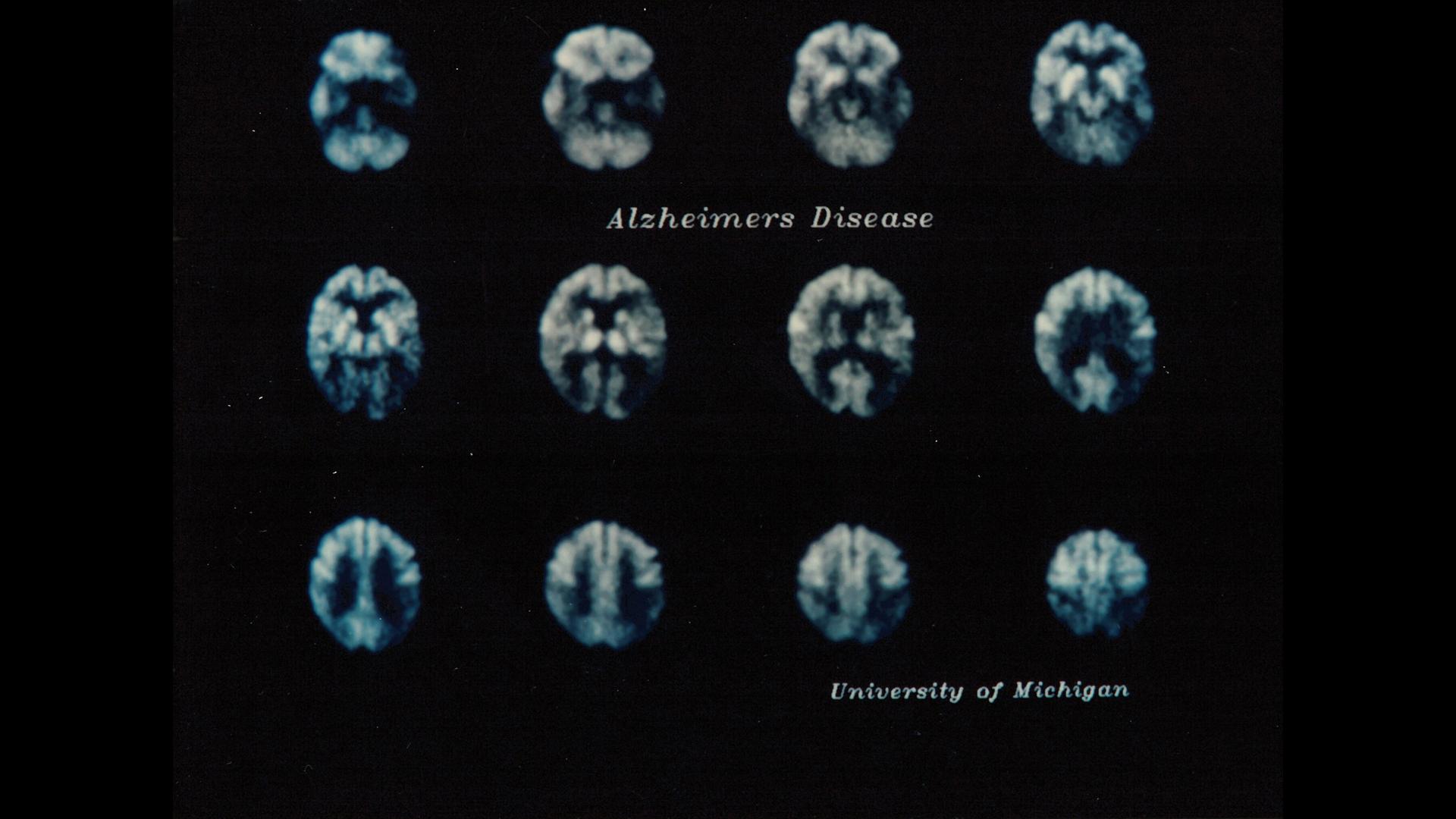
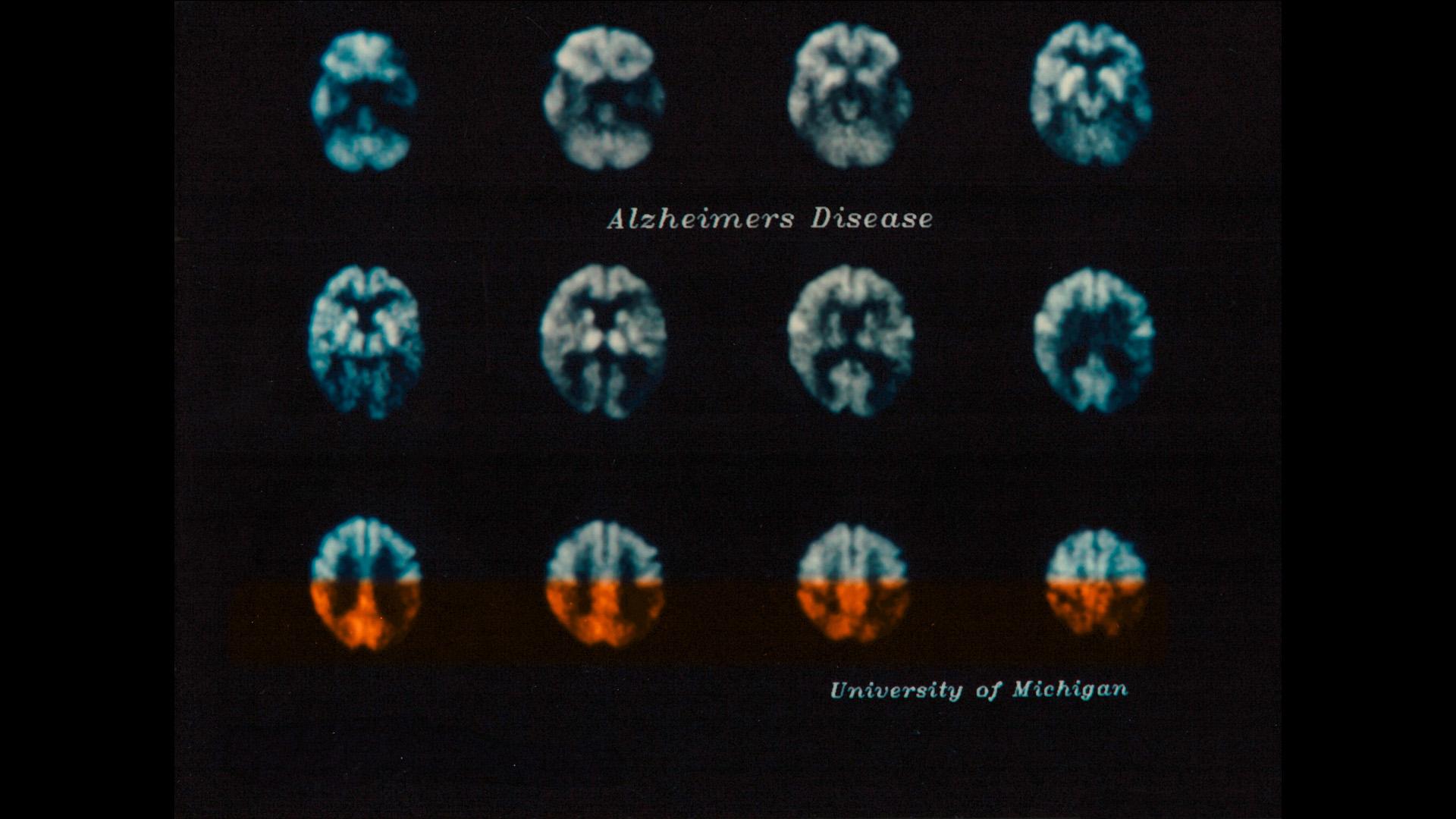
Die PET-Aufnahmen aus dem Jahr 1989 zeigen einen verminderten Glukoseverbrauch aufgrund der Störungen der Nervenzellfunktion in bestimmten Hirnregionen (Orange markiert), was auf eine Alzheimer-Krankheit hindeuten kann.
Die PET-Darstellung des Glukose-Stoffwechsel im Gehirn zeigt die Folgen, nicht aber die Ursachen der Alzheimer-Erkrankung. Das ändert sich Anfang der 2000er Jahre, als ein Forscherteam an der University of Pittsburgh mit der Entwicklung eines Tracers beginnt, der Beta-Amyloid-Plaques im Gehirn darstellt. Parallel dazu forscht bei Siemens ein Team von Wissenschaftler*innen an einem Biomarker, mit dem sich Tau-Ablagerungen identifizieren lassen. Mithilfe dieser Tracer und moderner PET-CT Geräte lässt sich Alzheimer heute bereits in einem frühen Stadium nachweisen, in dem das Gehirn noch nicht in einem fortgeschrittenen Stadium geschädigt ist. Doch was nützt die Früherkennung der Krankheit, wenn es keine Chance auf Heilung gibt?
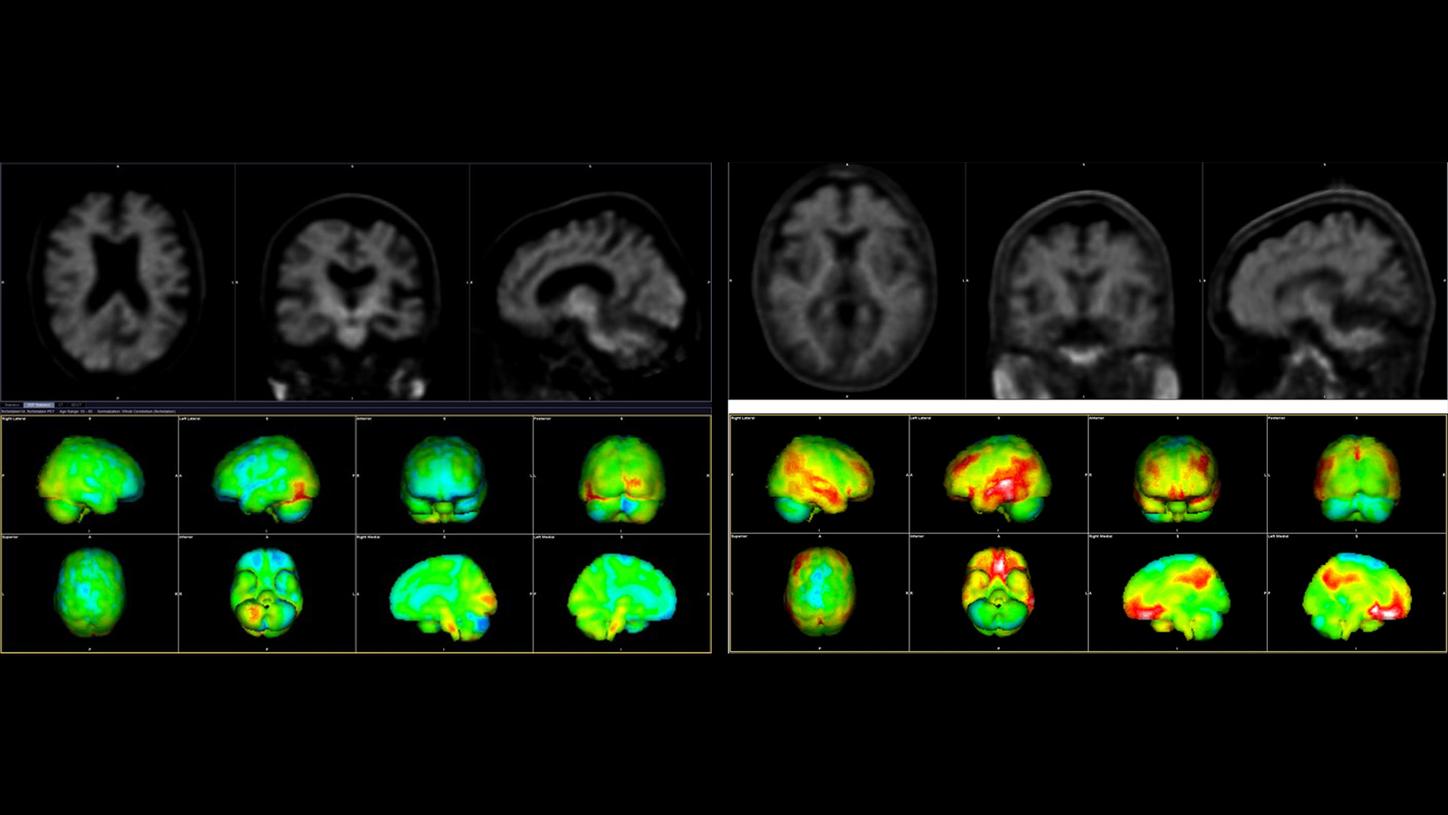
Amyloid PET-CT Aufnahmen zum Nachweis von Beta-Amyloid-Plaques (Rot markiert). Links ist das Gehirn einer gesunden älteren und rechts das einer an Alzheimer erkrankten Person zu sehen.
Data courtesy of Wentworth-Douglas Hospital, Dover, New Hampshire, USA
Ich beginne nun die Reise, die mich in den Sonnenuntergang meines Lebens führen wird.
Ronald Reagan, 1994
Mit diesen berührenden Worten beendet der ehemalige US-Präsident Ronald Reagan seinen Brief, mit dem er sich 1994 an die Öffentlichkeit wendet und seine Alzheimer-Erkrankung publik macht. Bis heute steht jedem, der die Diagnose „Alzheimer“ bekommt, diese Reise bevor, bei der man sich völlig verliert. Noch gibt es keine Heilung. Aber es gibt Hoffnung. Seit 2023 wurden in den USA zwei Antikörper-Wirkstoffe zugelassen, die sich gezielt gegen Beta-Amyloid-Plaques im Gehirn richten und diese auflösen.
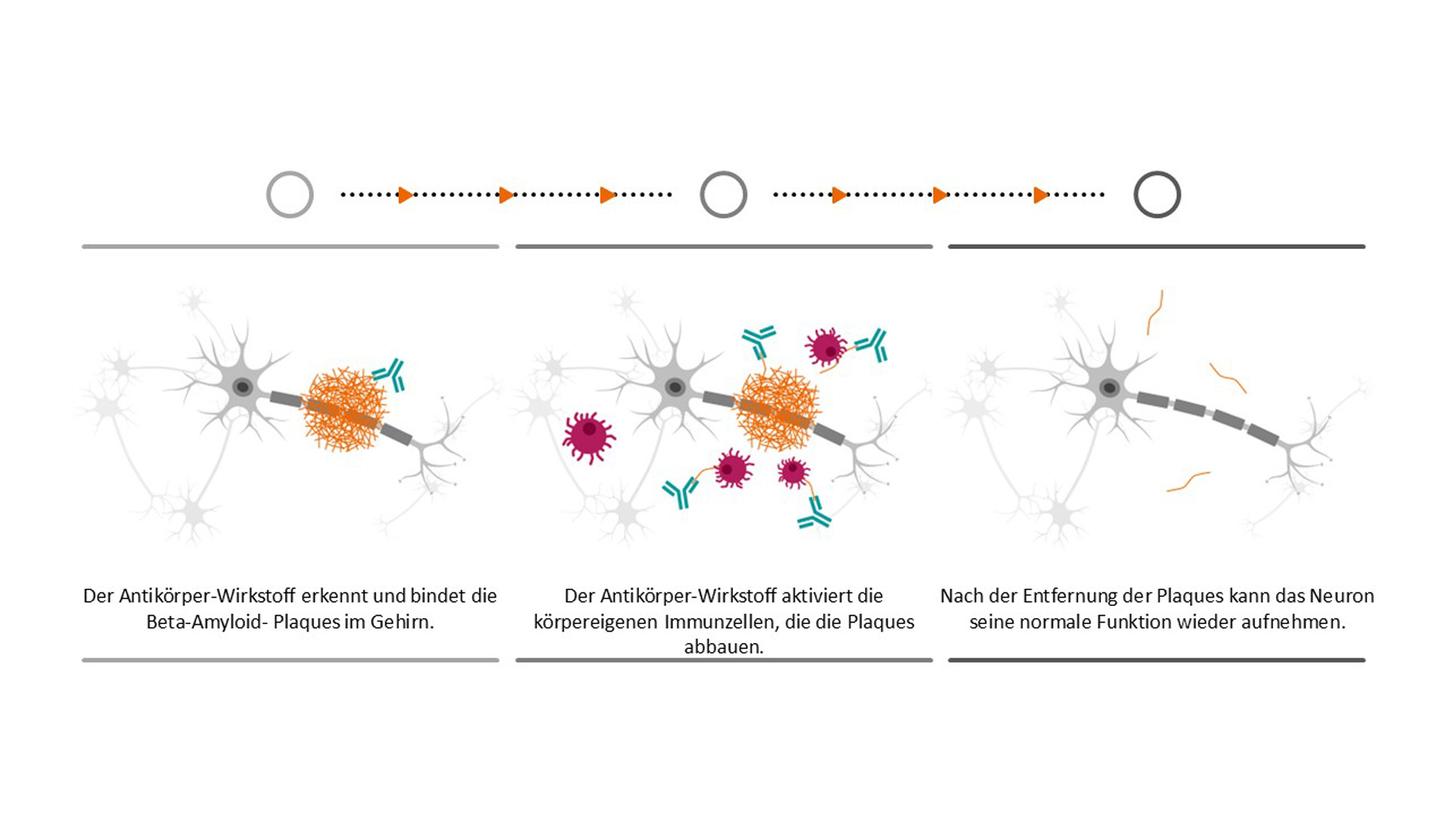
Die Wirkstoffe können die Erkrankung nicht heilen, sondern den Verlauf lediglich verlangsamen. Zudem kommen sie nur für eine kleine Patientengruppe in einem sehr frühen Stadium von Alzheimer in Frage. Und aufgrund vieler Nebenwirkungen muss der Verlauf der Therapie genau überwacht werden - es sind regelmäßige MRT-Scans nötig. Dennoch sind die Antikörper-Wirkstoffe ein Hoffnungsschimmer und nur eine von vielen Optionen, die momentan erforscht werden, um den Verlauf der Krankheit nicht nur zu verlangsamen, sondern sie irgendwann zu heilen. Im Mittelpunkt der Alzheimer-Forschung steht natürlich immer noch die Krankheit selbst, denn es gibt viele offene Fragen. Mit unseren Technologien unterstützen wir die Forschung und begleiten die Patient*innen auf ihrer Reise. Wir wollen dazu beizutragen, den Patient*innen mehr Zeit mit geliebten Menschen zu geben, in der sie möglichst lange selbstbestimmt nach ihren eigenen Vorstellungen leben können.
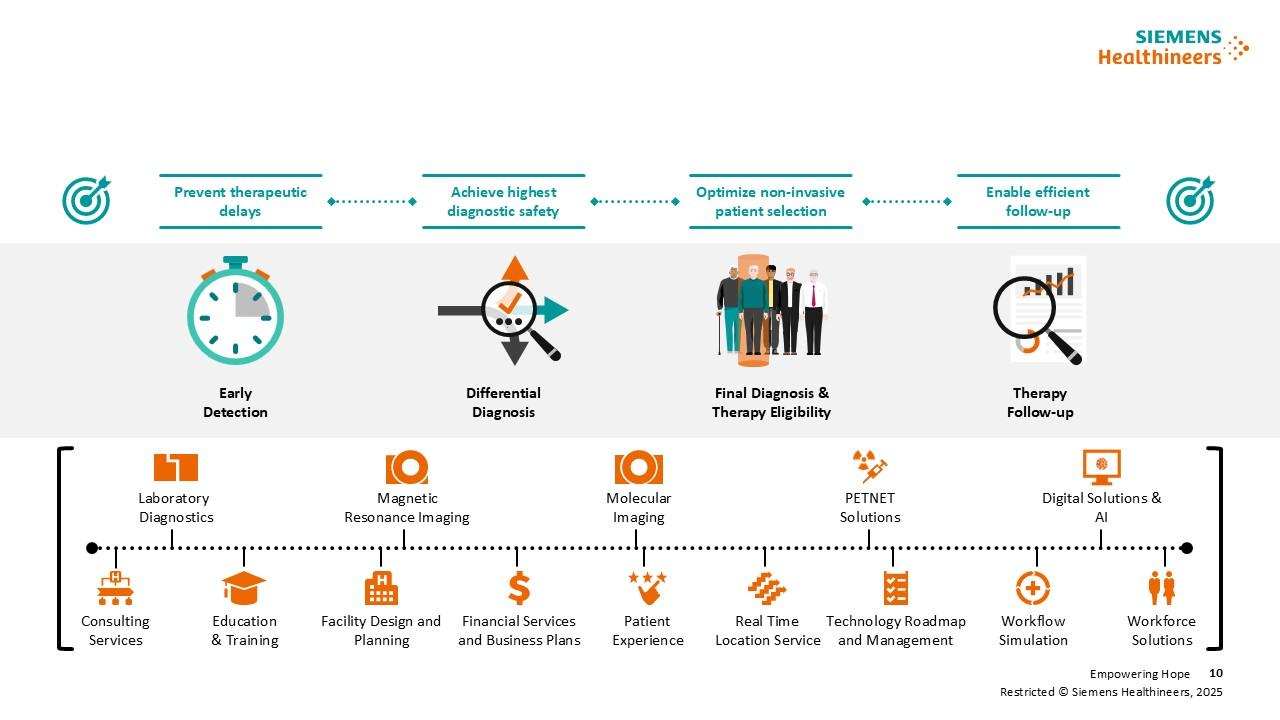
Die klinischen Lösungen von Siemens Healthineers unterstützen den gesamten Versorgungspfad bei Alzheimer: von der Früherkennung über die Differentialdiagnostik bis hin zur Therapiebegleitung.
Spezialistin für Historische Kommunikation und Historikerin im Siemens Healthineers Historical Institute





